由病毒感染引起的疾病给人类的生存和健康带来巨大威胁。天然免疫是宿主抵抗病毒感染的第一道屏障。受病毒刺激后,细胞会产生并分泌I型干扰素(Interferon, IFN),它们结合到细胞表面的干扰素受体(IFNAR1/2)上,激活转录因子STAT1、STAT2和IRF9,三者形成转录因子复合物进入细胞核启动干扰素刺激基因(Interferon-stimulated genes, ISGs)的表达,由众多的ISG来发挥抗病毒作用。然而病毒感染和IFN-I刺激会促进IFN-I 受体IFNAR1 的泛素化和降解,从而限制了IFN-I 的抗病毒功效。因此,维持IFNAR1 蛋白的稳定性对增强IFN-I 的抗病毒效果至关重要。
2021年6月23日,苏州大学生物医学研究院戴建锋教授团队在EMBO Reports上发表了题为 RNA-binding protein RBM47 stabilizes IFNAR1 mRNA to potentiate host antiviral activity 的研究成果。该研究首次阐明RBM47是一个ISG,且通过稳定IFNAR1 mRNA来增强宿主的抗病毒效应,提示了以RBM47为代表的RNA结合蛋白在宿主抗病毒天然免疫中发挥着重要作用。

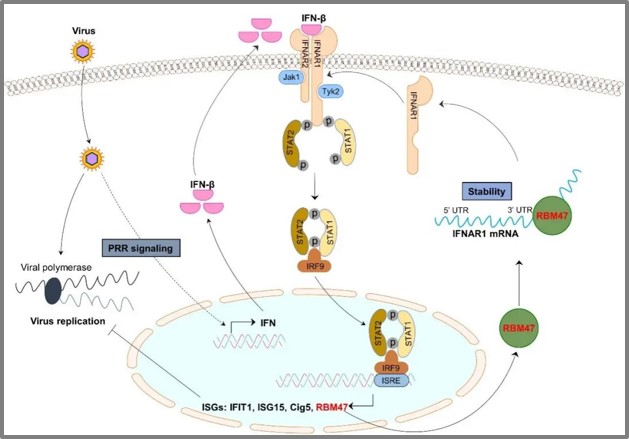
戴建锋教授团队在前期针对登革病毒(Dengue virus, DENV)的研究中发现,RBM47受DENV感染后表达上调,并具有抑制DENV复制的作用。进一步研究发现RBM47是一个ISG,受多种病毒诱导或干扰素刺激上调表达,且具有广谱的抗病毒作用。RBM47对IFN的产生没有明显作用,但对IFN应答元件ISRE的激活及ISGs的表达有显著增强效应。利用RNA结合蛋白免疫沉淀技术(RNA binding protein Immunoprecipitation, RIP),发现RBM47能特异性地结合I型干扰素受体IFNAR1 mRNA的3’-UTR,稳定了该基因的mRNA,继而提高细胞内IFNAR1的蛋白水平,促进病毒感染或干扰素诱导的STAT1/2的磷酸化,增强干扰素刺激基因ISGs的表达,放大宿主的抗病毒作用。
苏州大学生物医学研究院的戴建锋教授为本文的通讯作者,副教授王克振博士和博士生皇晨晓为该论文的共同第一作者。本研究得到国家自然科学基金和江苏省教育厅项目的资助。
原文链接:
https://www.embopress.org/doi/full/10.15252/embr.202052205
